Resumen
Objetivo: Presentar la respuesta clínica a largo plazo del tratamiento de un granuloma periférico de células gigantes en un implante oseointegrado en el maxilar inferior.
Caso clínico: Un paciente de 60 años, de sexo masculino, sin antecedentes sistémicos, concurrió por una lesión con márgenes definidos, de color rojizo morado y consistencia blanda sobre los tejidos blandos en la cara vestibular de un implante colocado en zona de 46. Se realizó la escisión quirúrgica de la lesión, se procesó el tejido extirpado y se envió al laboratorio. El estudio anatomopatológico confirmó el diagnóstico de granuloma periférico de células gigantes. La lesión recidivó dos veces. En la tercera extirpación se realizó la implantoplastía de la superficie del implante. La cicatrización no presentó inconvenientes. Hasta el último control, a los 5 años, no volvió a haber recidiva.
Conclusión: En este caso clínico, se logró mantener la salud periimplantaria durante 5 años luego de la eliminación de un granuloma periférico de células gigantes. No obstante, este tuvo que ser removido en tres oportunidades debido a la alta recidiva.
Palabras clave: Épulis de células gigantes, granuloma periférico de células gigantes, hiperplasia de células gigantes.
", "sameAs": "", "about": [ "Works", "Catalog" ], "pageEnd": "68", "pageStart": "74", "name": "Granuloma periférico de células gigantes asociado a un implante. Informe de un caso clínico con seguimiento a 5 años", "author":[ "Ezequiel Bolli" , "Guillermo Schinini" , "Hugo Romanelli" ] } ] }Autor/es: Ezequiel Bolli, Guillermo Schinini, Hugo Romanelli
Vol: 108 | Nº 2 | Ago 2020 | Páginas: 68-74
Presentado: 25/06/2020 | Aceptado: 15/08/2020 | Publicado: 30/08/2020
Stable URL: https://raoa.aoa.org.ar/revistas/?roi=1082000058 copiar
PDF | Citar este artículo | Volver
X Twitter | WhatsApp | Facebook | E-mail
CASO CLÍNICO - IMPLANTES
Granuloma periférico de células gigantes asociado a un implante. Informe de un caso clínico con seguimiento a 5 años
Implant-associated peripheral giant cell granuloma. A 5-year follow up case report
Presentado: 25 de junio de 2020
Aceptado: 15 de agosto de 2020
Ezequiel Bolli, Guillermo Schinini, Hugo Romanelli
Carrera de Especialización en Periodoncia, Universidad Maimónides, Buenos Aires, Argentina
Resumen
Objetivo: Presentar la respuesta clínica a largo plazo del tratamiento de un granuloma periférico de células gigantes en un implante oseointegrado en el maxilar inferior.
Caso clínico: Un paciente de 60 años, de sexo masculino, sin antecedentes sistémicos, concurrió por una lesión con márgenes definidos, de color rojizo morado y consistencia blanda sobre los tejidos blandos en la cara vestibular de un implante colocado en zona de 46. Se realizó la escisión quirúrgica de la lesión, se procesó el tejido extirpado y se envió al laboratorio. El estudio anatomopatológico confirmó el diagnóstico de granuloma periférico de células gigantes. La lesión recidivó dos veces. En la tercera extirpación se realizó la implantoplastía de la superficie del implante. La cicatrización no presentó inconvenientes. Hasta el último control, a los 5 años, no volvió a haber recidiva.
Conclusión: En este caso clínico, se logró mantener la salud periimplantaria durante 5 años luego de la eliminación de un granuloma periférico de células gigantes. No obstante, este tuvo que ser removido en tres oportunidades debido a la alta recidiva.
Palabras clave: Épulis de células gigantes, granuloma periférico de células gigantes, hiperplasia de células gigantes.
Abstract
Aim: To evaluate the long-term clinical response to the treatment of a peripheral giant cell granuloma in an osseointegrated implant in the lower jaw.
Clinical case: A 60-year-old male patient, with no systemic medical problems, presented a soft tissue lesion located at the buccal aspect of an implant placed in the 46 area. The lesion had defined reddish-purple margins and soft consistency. Surgical excision of the lesion was performed, processed and sent to the laboratory. The histopathology confirmed the diagnosis of peripheral giant cell granuloma. The lesion recurred twice. During the third surgical removal an implantoplasty of the implant surface was performed. The healing was uneventful and there was no recurrence until the last control at 5 years.
Conclusion: In this clinical case, perimplantar gingival health was maintained for 5 years after the surgical removal of a giant cell peripheral granuloma. However, it had to be removed three times, demonstrating a high recurrence.
Key words: Giant cell epulis, giant cell hyperplasia, peripheral giant cell granuloma.
Introducción
El granuloma periférico de células gigantes (GPCG) es una lesión benigna poco frecuente en la cavidad bucal. En un principio se asoció a piezas dentarias y rebordes edéntulos como una hiperplasia reactiva, que podía presentarse tanto en la encía como en la mucosa alveolar, como respuesta a una irritación local o trauma crónico.1 En algunas ocasiones involucra al hueso subyacente, provocando una reabsorción ósea superficial de poca magnitud. Tiene mayor predilección por el sexo femenino, así como por el maxilar inferior cuando se encuentra asociado a piezas dentarias. Afecta más frecuentemente a la encía vestibular que a la lingual o a la palatina. En cuanto a su localización anterior o posterior, Regezzi et al.2 informan que mayormente se localiza en las áreas incisiva y canina, mientras que Bodner et al.3 encuentran que es más común en las regiones premolar y molar. La edad de aparición es variable, aunque suele aparecer entre la cuarta y la sexta década de la vida.
El GPCG ha sido llamado tumor de células gigantes, osteoclastoma, granuloma reparativo periférico de células gigantes, épulis de células gigantes e hiperplasia de células gigantes. En un principio se lo consideró una lesión de origen neoplásico, hasta que Jaffe4 propuso que se trataba de una respuesta reactiva de los tejidos. Bernier y Cahn,5 al observar su presencia tanto en la encía como en el hueso alveolar, distinguieron un tipo periférico y otro central. Años después se identificó la asociación entre la lesión y factores irritantes como exodoncias, infecciones crónicas, prótesis desajustadas, el uso de palillos dentales y, últimamente, los implantes.6-9 Shafer et al.6 señalaron que se trata de una respuesta proliferativa anormal de los tejidos ante un trauma.
Se cree que se origina a partir del periostio o ligamento periodontal, tras una irritación o un traumatismo crónico que actúa localmente.10 Se observa como un nódulo bien delimitado, de color rojo, azul o morado, con base sésil o pediculada, consistencia blanda o firme y superficie lisa o lobular y, en ocasiones, con ulceraciones.2 Puede presentar hemorragia a la palpación.6 El tamaño varía de 0,5 a 1,5 cm, aunque se han informado lesiones de hasta 5 cm; no obstante, las lesiones mayores a 2 cm son menos frecuentes.11
El tiempo de evolución va de 3 meses a 4 años.12
En general, el GPCG es una lesión asintomática, a no ser que exista un trauma constante durante la masticación o presente ulceración.13 El diagnóstico es histopatológico, ya que clínicamente es similar a otras lesiones, como el granuloma piógeno, el fibroma osificante periférico o el fibroma odontogénico periférico. Por sus características histológicas, también se considera para el diagnóstico diferencial a la lesión central de células gigantes (LCCG) y al tumor pardo del hiperparatiroidismo.14
Suelen asociarse a dientes. Su vinculación a tejidos periimplantarios ha sido escasamente informada en la literatura. 8, 15
Se ha demostrado que existe una alta probabilidad de recidiva de estas lesiones sobre dientes e implantes, y que en estos últimos es aún mayor. El índice de recidiva sobre dientes informado en la literatura es del 10%,16, 17 mientras que sobre implantes es considerablemente mayor.18
El tratamiento consiste en la escisión quirúrgica local, procurando eliminar toda la base de la lesión y el curetaje del hueso subyacente. Además, se deben identificar y eliminar los factores irritantes locales, tales como las espiras de implantes de tratamiento rugoso expuestas al medio bucal.2
Dado que la bibliografía sobre GPCG en implantes es escasa, aún no contamos con un protocolo de tratamiento basado en evidencia científica suficiente.1 El objetivo de este artículo es presentar el trata- miento quirúrgico de un caso clínico de GPCG asociado a un implante y su seguimiento a 5 años.
Caso clínico
Un paciente de 60 años, de sexo masculino, sin antecedentes sistémicos, consultó en 2014 por una inflamación crónica sobre los tejidos adyacentes a un implante de hexágono externo y cuello pulido de 5 × 11,5 mm (B&W, Buenos Aires, Argentina) colocado en 2006 sobre hueso nativo, en zona de pieza 46. La ubicación tridimensional era correcta, pero durante su colocación parte de una espira por vestibular del implante quedó expuesta por ausencia de tejido óseo y fue cubierta por mucosa queratinizada.
A 4 meses de su colocación, se rehabilitó con una corona ceramometálica atornillada (fig. 1). Durante los 8 años posteriores, no presentó alteraciones en los tejidos periimplantarios. En 2014 se registró una lesión nodular, sésil, bien delimitada, de color rojizo morado, de 7 mm de ancho por 5 mm de alto, ubicada por vestibular del implante (fig. 2).
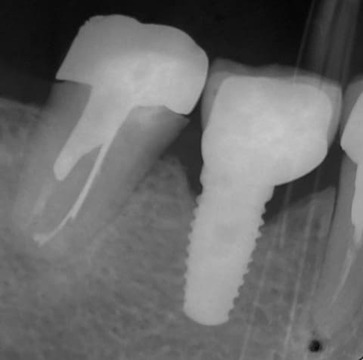
Figura 1. Radiografía de la corona metalocerámica instalada en 2006.
Luego de la firma del consentimiento informado, se procedió a la escisión de la lesión con bisturí 15C (Swann-Morton, Sheffield, Reino Unido) y al curetaje óseo de la zona afectada. Al momento de la cirugía, se observaron dos espiras expuestas por vestibular (fig. 3). Se indicó colutorio (10 ml de digluconato de clorhexidina al 0,12%) dos veces al día por 5 días y se controló su evolución una vez por semana durante un mes. La imagen clínica y radiográfica fue satisfactoria (figs. 4-5). La lesión se colocó en un recipiente con formol al 10% y fue remitida a la cátedra de Anatomía Patológica de la Universidad de Buenos Aires para su análisis. El resultado anatomopatológico confirmó la presencia de un GPCG.
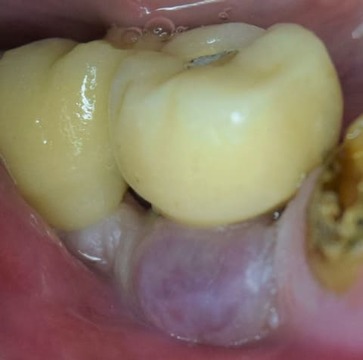
Figura 2. Primera aparición del GPCG en 2014.
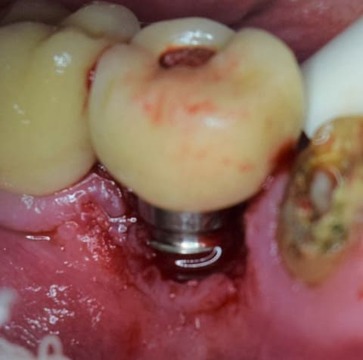
Figura 3. Primera extirpación de la lesión con bisturí.
A fines del mismo año, el paciente consultó nuevamente por una lesión similar a la anterior pero de mayor tamaño (9 mm de ancho por 7 mm de alto) y ulcerada. Se decidió su extirpación mediante el uso del láser de diodo iLase® (BioLase, Irvine, CA, Estados Unidos) y se controló de la misma manera que la vez anterior (figs. 6-8).
Un año más tarde, en 2015, la lesión recidivó con unas dimensiones aún mayores (12 mm de ancho por 9 mm de alto) (figs. 9-10). Se procedió a una nueva intervención quirúrgica en la que se efectuó la remoción de la lesión con bisturí, aunque en esta oportunidad se efectuó con un margen de seguridad de 1 mm. Se elevó un colgajo mucoperióstico para acceder al curetaje del hueso subyacente y a la superficie del implante. Se registró una importante reabsorción ósea, 5 espiras por vestibular y de 2 a 3 por proximal.
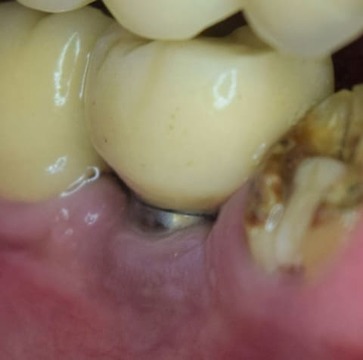
Figura 4. Cicatrización posquirúrgica.
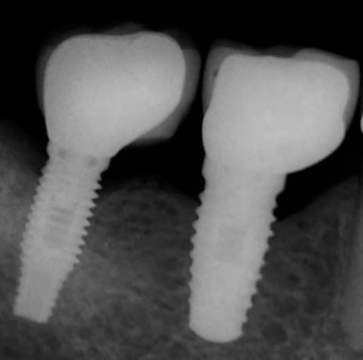
Figura 5. Radiografía preoperatoria de la segunda intervención quirúrgica.
Teniendo en cuenta la alta tasa de recidiva y la exposición de espiras, se tomó la decisión de realizar una implantoplastía (modificación anatómica de la superficie expuesta del implante). Se removieron las espiras expuestas con sistema rotatorio a alta velocidad e irrigación abundante con fresa redonda de carburo de tungsteno CAH 1.027 (Komet Dental, Lemgo, Alemania), seguida de una preparación a baja velocidad con irrigación externa y fresa redonda de carburo de tungsteno RA6 de 1,8 mm (Komet Dental) para quitar la mayor cantidad de imperfecciones producidas por el sistema de alta velocidad (fig. 11). Por último, mediante goma dura de composite del kit de pulido de resinas y amalgamas Kenda Complete® (Kenda Dental Polishers, Vaduz, Liechtenstein), se procedió al pulido final. Se reposicionó el colgajo y se prescribió la colocación de gel de clorhexidina al 1% en la zona. Se retiró la sutura a los 15 días y se controló quincenalmente durante 2 meses (fig. 12).
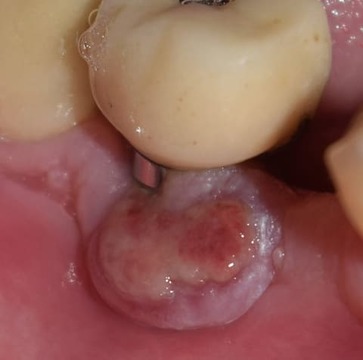
Figura 6. Recidiva de la lesión un año después de la primera intervención.
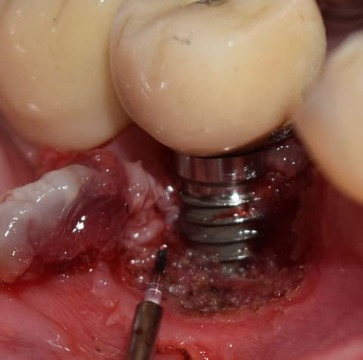
Figura 7. Eliminación con láser de diodo iLase® (BioLase).
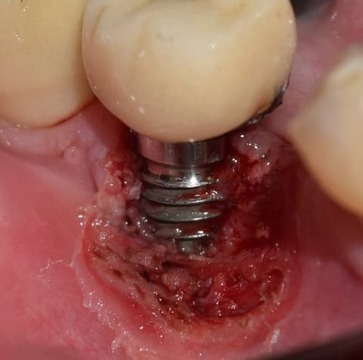
Figura 8. Extirpación total de la lesión.
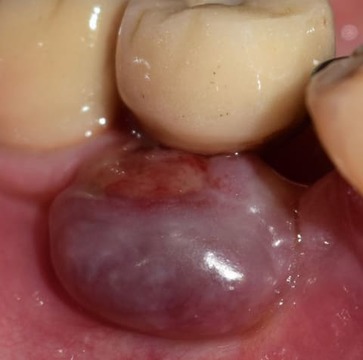
Figura 9. Segunda recidiva del GPCG.
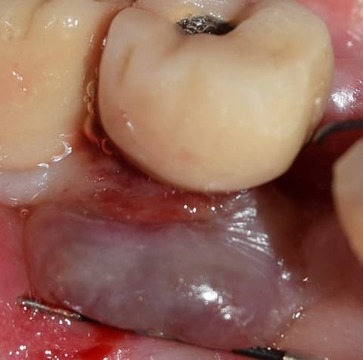
Figura 10. Medición del tamaño del GPCG.
Se monitoreó al paciente por 5 años, a lo largo de los cuales se corroboró, clínica y radiográficamente, su salud periimplantar. El paciente mantuvo una adecuada higiene y se realizaron controles periódicos (figs. 13-14).
Discusión
Aunque la etiología precisa del GPCG es desconocida, es considerada una lesión reactiva inducida por trauma o irritación. La tasa de recurrencia en implantes es elevada, por lo tanto se recomienda eliminar la lesión completamente, desde su base, con amplio margen de seguridad, realizar el curetaje óseo, detoxificar la superficie expuesta del implante y, de ser necesario, reemplazar la prótesis. Estas maniobras podrían ser suficientes para prevenir la recidiva. Sin embargo, algunos autores sostienen que la resolución de la lesión se obtendría con la remoción del implante. 8 , 18 En nuestro reporte se optó por el método más conservador, manteniendo el implante en boca.
El GPCG presenta un patrón de comportamiento agresivo que involucra al hueso subyacente. Sin embargo, existe controversia acerca de si la pérdida ósea marginal alrededor del implante sería la causa o la consecuencia del GPCG. En este caso, se realizó la implantoplastía de las espiras expuestas una vez eliminada la lesión, tratando de dejar la superficie en contacto con la mucosa periimplantaria lo más lisa y pulida posible. Cloutier et al., en 2007, sugirieron que con el tiempo la superficie abrasiva del implante tendría la capacidad de transformarse en una fuente de irritación crónica que podría producir lesiones reactivas, como granulomas piógenos y GPCG.19
Los resultados de este caso clínico nos llevan a interpretar que la recidiva de la lesión probablemente se deba a la escisión incompleta y/o a la persistencia de los factores irritativos causales. Por ese motivo, se realizó la eliminación del GPCG desde la base de la lesión, además de un minucioso curetaje óseo y la modificación anatómica de la superficie del implante. Consideramos que todo esto podría contribuir a la efectividad del tratamiento a largo plazo, disminuyendo su alta tasa de recidiva. No obstante, debido a la escasa evidencia científica de GPCG en relación con implantes oseointegrados y a la ausencia de un protocolo quirúrgico establecido, los resultados clínicos obtenidos en el presente informe deberían interpretarse con precaución.
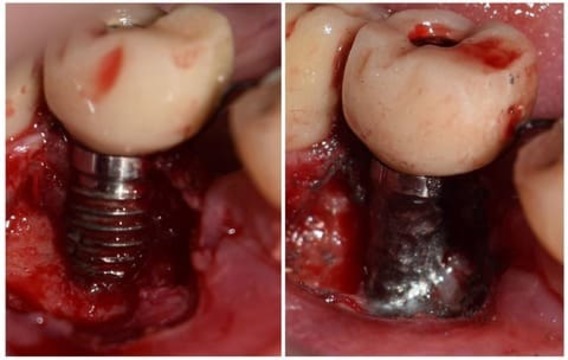
Figura 11. Extirpación completa de la lesión e implantoplastía de las espiras expuestas.
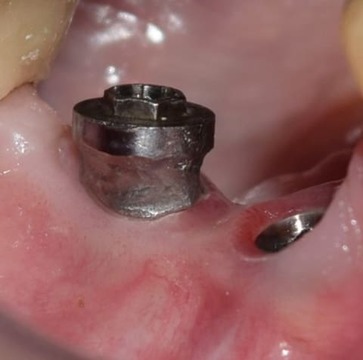
Figura 12. Control a los 2 meses.
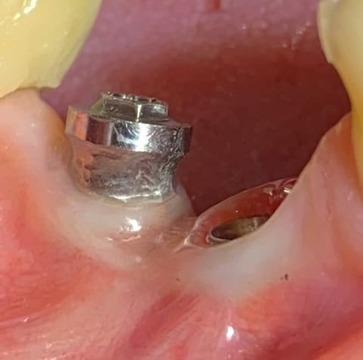
Figura 13. Control clínico de los tejidos periimplantarios a 5 años.
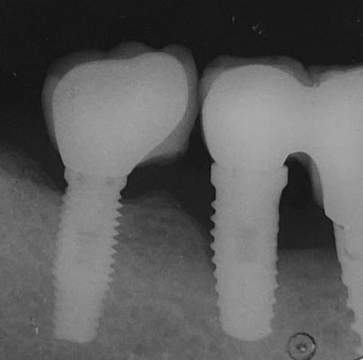
Figura 14. Radiografía de control a 5 años. Nótese la pérdida ósea alrededor del implante en 46 en comparación con lo que se observa en la figura 1.
Conclusión
En este caso clínico se logró mantener la salud periimplantaria durante 5 años luego de la remoción de un GPCG. No obstante, este tuvo que ser removido en tres oportunidades, demostrando una alta recidiva.
Los autores declaran no tener conflictos de interés en relación con este artículo y afirman no haber recibido financiamiento externo para realizarlo.
Contacto:
Ezequiel Bolli
ezequielbolli@hotmail.com
Cervantes 290, Belén de Escobar (B1625KSE9)
provincia de Buenos Aires, Argentina
1. Scarano A, Iezzi G, Artese L, Cimorelli E, Piatelli A. Peripheral giant cell granuloma associated with a dental implant. A case report. Minerva Stomatol 2008;57:529-34.
2. Regezzi JA, Scuibba JJ, Jordan R. Oral pathology clinical pathologic correlations. 6a ed., St Louis, Elsevier, 2012, pp. 150-1.
3. Bodner L, Peist M, Gatot A. Growth potential of peripheral giant cell granuloma. Oral Surg Oral Med Oral Pathol 1995;83:548-51.
4. Jaffe HL. Giant-cell reparative granuloma, traumatic bone cyst, and fibrous (fibro-osseous) dysplasia of the jawbones. Oral Surg Oral Med Oral Pathol 1953;6:159-75.
5. Bernier JL, Cahn LR. The peripheral giant cell reparative granuloma. J Am Dent Assoc 1954;49:141-8.
6. Shafer WG, Hine MK, Levy BM. Tratado de patología bucal. 3a ed., México, Interamericana, 1974, pp. 132-3.
7. Breault LG, Fowler EB, Wolfgang MJ, Lewis DM. Peripheral giant cell granuloma. A case report. Gen Dent 2000;48:716-9.
8. Hirshberg A, Kozlovsky A, Schwartz-Arad D, Mardinger O, Kaplan I. Peripheral giant cell granuloma associa- ted with dental implants. J Periodontol 2003;74:1381-4.
9. Bischof M, Nedir R, Lombardi T. Peripheral giant cell granuloma associated with a dental implant. Int J Oral Maxillofac Implants 2004;19:295-9.
10. Chaparro-Avendaño AV, Berini-Aytes L, Gay-Escoda C. Peripheral giant cell granuloma. A report of five cases and review of the literature. Med Oral Patol Oral Cir Bucal 2005;10:48-57.
11. Kfir Y, Buchner A, Hansen LS. Reactive lesions of the gingiva. A clinicopathological study of 741 cases. J Periodontol 1980;51:655-61.
12. Amish D, Jyoti M, Kinjal R, Hiren P. Case report mana- gement of peripheral giant cell granuloma in 4 1/2 year old child-a case report. Oral Heal Res 2011;2:79-84.
13. Vergara HC, Caballero AD, Arévalo LA. Granuloma periférico de células gigantes. Reporte de un caso clínico. Rev Fac Odontol Univ Antioquia 2010;22:117-21.
14. McCarthy PL. Diseases of the oral mucosa. 2a ed., Filadelfia, Lea & Febiger, 1980, pp. 433-4.
15. Olmedo D, Paparella ML, Brandizzi D, Cabrini R. Reactive lesions of periimplant mucosa associated with titanium dental implants: a report of 2 cases. Int J Oral Maxillofac Surg 2010;39:503-7.
16. Miguell AJ, Robinson PA, Hume WJ. Peripheral giant cell granuloma: a clinical study of 77 cases from 62 patients and literature review. Oral Dis 1995;1:12-9.
17. Brown A, Camargo de Moraes P, Sperandio M, Borges Soares A, Cavalcanti Araujo V, Passador-Santos F. Peripheral giant cell granuloma associated with a dental implant: a case report and review of the literature. Case Rep Dent 2015;ID697673. Disponible en: dx.doi.org/10.1155/2015/697673
18. Hernández G, López-Pintor RM, Torres J, Vicente J. Clinical outcomes of periimplant peripheral giant cell granuloma: a report of three cases. J Periodontol 2009;80:1184-91.
19. Cloutier M, Charles M, Carmichael RP, Sandor G. An analysis of peripheral giant cell granuloma associated with dental implant treatment. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2007;103:618-22.
X Twitter | WhatsApp | Facebook | E-mail

Las obras publicadas en este sitio están bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional
















Los artículos científicos de RAOA se identifican con DOI (Digital Object Identifier) Crossref.
Visitas al artículo: 4.439

Lecturas en línea: 4.068

Descargas del artículo: 371

Accesos RAOA Id: 422

Database ID: 2023001001
Épulis de células gigantes granuloma periférico de células gigantes hiperplasia de células gigantes Giant cell epulis giant cell hyperplasia peripheral giant cell granuloma





La Revista de la Asociación Odontológica Argentina, RAOA, es la principal vía de expresión de la producción científica argentina en odontología y un vínculo de unión y medio de información para los colegas e instituciones del país y del exterior.
Versión impresa ISSN 0004-4881
Versión electrónica ISSN 2683-7226.
DOI: 10.52979/raoa.1898
Título abreviado: Rev Asoc Odontol Argent