Vidrios bioactivos en endodoncia. Revisión narrativa de sus propiedades biológicas
Bioactive glasess in endodontics. A narrative review about their biological properties
MATERIALES DENTALES | REVISIÓN NARRATIVA | OPEN ACCESS | PEER-REVIEWED
Vidrios bioactivos en endodoncia. Revisión narrativa de sus propiedades biológicasBioactive glasess in endodontics. A narrative review about their biological properties
Autor/es: Osvaldo Zmener
Vol: 112 | Nº 1 | elocation Id: e1120451
Presentado: 20/12/2023 | Aceptado: 11/01/2024 | Publicado: 15/03/2024
DOI: https://doi.org/10.52979/raoa.1120451.1248 copiar
PDF | Citar este artículo | Volver
X Twitter | WhatsApp | Facebook | E-mail
REVISIÓN NARRATIVA - MATERIALES DENTALES
Vidrios bioactivos en endodoncia. Revisión narrativa de sus propiedades biológicas
Bioactive glasess in endodontics. A narrative review about their biological properties
Presentado: 20 de diciembre de 2023
Aceptado: 11 de enero de 2024
Publicado: 15 de marzo de 2024
Osvaldo Zmener

Carrera de Especialización en Endodoncia, Escuela de Odontología USAL/AOA, Facultad de Medicina, Universidad del
Salvador, Buenos Aires, Argentina
Resumen
Los vidrios bioactivos (VBa) son materiales biocerámicos que tienen una extensa aplicación en medicina y odontología.
A causa de su contenido de calcio y fosfato son muy similares a la hidroxiapatita del tejido óseo. Su biocompatibilidad y bioactividad los hacen materiales muy útiles para ser aplicados en diferentes áreas de la práctica dental, tales como periodoncia, cirugía, odontología restauradora y endodoncia.
En endodoncia los VBa están indicados para realizar protecciones pulpares directas, pulpotomías, desinfecciones y obturaciones del sistema de conductos radiculares. El objetivo del presente trabajo fue realizar una revisión de las propiedades biológicas de los VBa en relación a sus aplicaciones en endodoncia.
Palabras clave: Biocompatibilidad, Bioglass®, hidroxiapatita, vidrio bioactivo.
Abstract
Bioactive glasses (BGs) are bioceramic materials with extensive clinical applications in medicine and dentistry. Because of their phosphate and calcium contents, they are like the hydroxyapatiteof bone tissue. Their biocompatibility and bioactivity make them very useful biomaterials in different areas of dental practice, such as periodontics, oral surgery, restorative dentistry, and endodontics. In endodontics, bioactive glasses are indicated for direct pulp capping, pulpotomies, disinfections and fillings of the root canal system. The aim of this work was to carry out a review of the biological properties of BGs in relation to its application in endodontics.
Key words: Bioactive glass, biocompatibility, Bioglass®, hydroxyapatite.
Introducción
Durante los últimos 30 años, la investigación en el área de los materiales dentales se ha extendido considerablemente, especialmente con referencia a los materiales bioactivos (MBa). Los MBa tienen la particularidad de generar una respuesta biológica de los tejidos con los que se ponen en contacto. Algunos materiales de tipo natural (colágeno, fibrina o ácido hialurónico) así como también sintéticos orgánicos (policaprolactona) o inorgánicos (hidroxiapatita o diferentes composiciones de silicatos o fosfatos) han sido investigados para su aplicación en el área experimental de la ingeniería de los tejidos dentales.(1) La investigación en el campo de los biomateriales se ha enfocado particularmente en la regeneración de tejidos y en ese sentido, los vidrios bioactivos (VBa) son los biomateriales que han despertado más interés en los profesionales del área de la medicina y la odontología.(2)
La acción de los VBa se basa en la presencia de silicatos estructurados dentro de una red tridimensional de sílice que, en contacto con los fluidos tisulares tiene la capacidad de unirse químicamente tanto con los tejidos blandos como con los tejidos mineralizados mediante la formación de cristales de hidroxiapatita.(3-5 )
Esto se produce como consecuencia de la liberación de importantes proporciones de iones Ca, P, Si y Na(6,7) durante su degradación en los tejidos (característica específica del material para iniciar el proceso bioactivo). Con un módulo de elasticidad que puede variar entre 30 y 50 MPa (muy cercano al del tejido óseo natural), los VBa son compatibles, osteogénico y osteoconductivo.(8) Tiene acción antibacteriana, baja solubilidad, y su radiopacidad es superior a 3,0 mm en la escala de aluminio requerida por la norma ISO 6876 para materiales endodónticos.(9) Presenta un pH cercano a 10,5 y provee un efectivo sellado en la interfaz material-tejido mineralizado, razón por la que ha sido sugerido como material con amplias posibilidades de uso en endodoncia.(9-14)
La introducción de modificaciones en su composición química ha permitido que los VBa puedan ser aplicados en diferentes áreas de la odontología. El Bioglass® (University of Florida, Estados Unidos) es uno de los principales exponentes entre otras variedades aprobadas para su uso experimental y clínico por la US Food and Drugs Administration (FDA).
El Bioglass® se comercializa en forma de polvo o en partículas (fig.1) y también con el nombre de PerioGlas® o Nova Bone.® Estos dos últimos están especialmente indicados como relleno para defectos periodontales con pérdida ósea o para casos que requieren cirugía periradicular.(15) En cuanto a su contenido de calcio y fosfato, los VBa son similares a la hidroxiapatita ósea y tiene la capacidad de estimular la proliferación y diferenciación de osteoblastos e iniciar la síntesis y aposición de la matriz orgánica ósea.(16) En la presentación polvo/líquido del Bioglass ® el polvo está compuesto por dióxido de silicio (45%), óxido de sodio (24,5%), óxido de calcio (24,5%) y pentóxido de fósforo (6%), con el agregado de otros minerales bioactivos como fluorapatita, wallactonita y fosfato tricálcico. El líquido provisto para incorporar al polvo es generalmente buffer fosfato o buffer fosfato con la adición de 1% de gel de alginato de sodio.(17,18)

Figura 1. Microfotografía de partículas de Bioglass® sobre la superficie de una muestra ex vivo de dentina humana. Microscopía electrónica de barrido (Magnificación original X8000; Barra= 5μm).
Los Vba han demostrado una actividad antibacteriana efectiva frente a diferentes cepas microbianas tales como Enterococcus faecalis, A. actinomycetemcomitans, Porphyromonas gingivalis, Actinomyces naeslundi, Streptococcus mutans, Streptococcus sanguis, Actinomyces viscosus, Fusobacterium nucleatum, Provotella intermedia, Lactobacillus casei y Escherichia coli,(10,11,19-25) especialmente a causa de la alcalinización del medio a partir de la disolución del material, la posible interacción con la dentina y la presión osmótica de las áreas circundantes. En sus diferentes combinaciones, el Bioglass® es un material biocompatible y bioactivo(8,11,25-27) y en endodoncia ha sido especialmente indicado para ser utilizado en casos de protecciones pulpares directas,(28-33) pulpectomías y pulpotomías, así como también para la desinfección y obturación del sistema de conductos radiculares.(10, 22) El objetivo del presente trabajo fue realizar una revisión de las propiedades biológicas de los VBa en relación a sus aplicaciones en endodoncia.
Desarrollo
Protección pulpar directa
Experiencias en animales
En 1993, Oguntebi et al.(28) utilizaron por primera vez Bioglass® en protecciones pulpares directas en 48 piezas dentarias sanas de 4 cerdos. Compararon la respuesta de la pulpa con otros materiales tales como muestras de dentina autóloga descalcificada o un material a base de hidróxido de calcio fraguable (Life®; Kerr, Romulus MI, Estados Unidos). Luego de 90 días realizaron micro radiografías y secciones histológicas y comprobaron que la reparación por medio de nuevo tejido calcificado de tipo tubular fue significativamente superior en los casos tratados con Bioglass®, donde incluso no se observaron áreas de necrosis. Dos años más tarde, Oguntebi et al.(29) realizaron un estudio cuantitativo midiendo el espesor de los puentes dentinarios formados a partir de protecciones pulpares directas en dientes de cerdo con Bioglass®, dentina descalcificada, Life® o Teflón®. Los autores analizaron imágenes computarizadas de micro radiografías. Si bien los casos donde se utilizó Bioglass® presentaron puentes dentinarios de mayor espesor, también sugirieron que independientemente del tipo de material de protección, parecería ser más importante para el proceso reparativo la acción ejercida por los componentes de la matriz extracelular de la dentina.
Long et al.(30) realizaron protecciones pulpares directas en molares de ratas y comprobaron que el Bioglass® estimulaba la reparación de la herida pulpar mediante la formación de puentes dentinarios completos y sin interrupciones. Hanada et al.(31) analizaron in vitro la capacidad del Bioglass® de inducir la formación de cristales de hidroxiapatita e in vivo la formación de dentina reparativa en exposiciones pulpares también realizadas en molares de rata. Para la experiencia in vitro utilizaron cultivos de células similares a odontoblastos en contacto con probetas de Bioglass® sobre las que se observó la formación de cristales de hidroxiapatita. En la experiencia in vivo, el Bioglass® indujo la formación de dentina reparativa mediada por nuevos odontoblastos cuya identidad fue comprobada mediante la expresión de marcadores específicos de odontoblastos en el área de la exposición pulpar.
En base a los resultados, los autores determinaron que los cementos a base de Bioglass® pueden ser utilizados como material de protección directa de la pulpa expuesta. En un ensayo piloto (Zmener y Canzobre, 2023; datos no publicados) se llevaron a cabo protecciones pulpares directas en ratas con un cemento experimental que contiene un 37% de Bioglass® en su formulación; y luego de 34 días, los autores observaron la formación de un tejido calcificado (puente dentinario) y la conservación de la pulpa vital (fig.2).
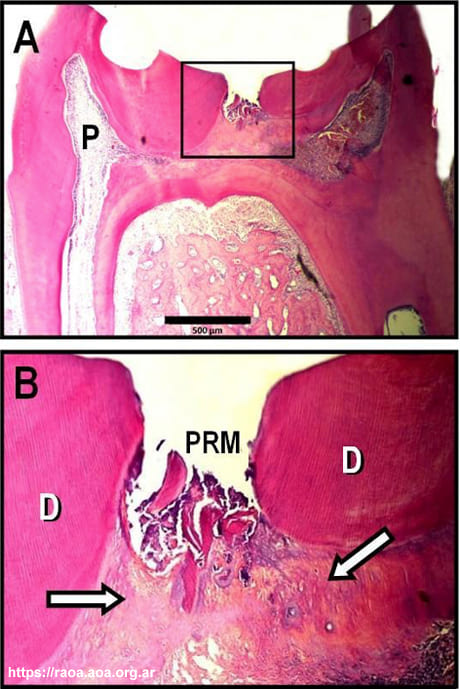
Figura 2. A: Microfotografía de una sección histológica perteneciente a un primer molar inferior de rata, en el que se realizó una exposición pulpar experimental y la protección con un cemento experimental que contiene un 37% de Bioglass®. Se observa un tejido calcificado (puente dentinario) que repara el defecto (P: La pulpa se encuentra vital. Hematoxilina y eosina; magnificación original X20; barra= 500 μm). B: Mayor aumento del área del recuadro en A. Se observa el puente dentinario (indicados con flechas) con algunas inclusiones celulares (PRM: Partículas dentinarias mezcladas con restos del material de protección, D: Dentina. Hematoxilina y eosina; magnificación original X100).
Experiencias clínicas en humanos
Las experiencias clínicas en humanos son escasas. En 2016, Haghgoo y Ahmadvant(32) realizaron protecciones pulpares directas con MTA o Bioglass® en 11 caninos primarios que debían ser extraídos por razones ortodóncicas. Luego de 60 días, los dientes fueron extraídos y preparados para su estudio histológico. Se observó la formación de puentes dentinarios completos y normalización del tejido pulpar en todos los casos y no se registraron diferencias significativas en los resultados de las protecciones realizadas con ambos materiales. Dos años más tarde, Haghgoo et al.(33) repitieron la experiencia clínica en 20 caninos primarios que también debían ser extraídos por razones ortodóncicas y confirmaron que el Bioglass presenta un excelente comportamiento como material de protección pulpar directa.
Obturación del sistema de conductos radiculares
En la última década, los VBa han sido investigados sobre su posible uso como material de obturación. Con ese objetivo, se han desarrollado diferentes formulaciones experimentales y comerciales.(34) GuttaFlow ® bioseal (Coltene/WhaledentGmBH, Langenau, Suiza) es un material que contiene VBa en su composición y cuyas propiedades biológicas han sido exhaustivamente investigadas.(35) GuttaFlow® 2 (Coltene/Whaledent) es otra versión del material que combina polvo de gutapercha y sellador (dos en uno).
Ambos selladores están compuestos por gutapercha, polydimetylsiloxano (PDS), dióxido de circonio, Bioglass® y un catalizador. De acuerdo a la información provista por el fabricante, GuttaFlow® bioseal presenta un tiempo de trabajo de 5 minutos y polimeriza en un período de 12 a 16 minutos. GuttaFlow® 2 tiene un tiempo de trabajo más extenso (entre 10 y 15 minutos) y polimeriza entre los 25 y los 30 minutos. Ambos materiales presentan una ligera expansión luego de la polimerización, baja solubilidad, liberan adecuadas proporciones de calcio, alcalinizan el medio, tienen capacidad de incorporarse a la dentina, son biocompatibles y permiten obtener obturaciones de gran calidad tal como lo demostraran Zhong et al.(42) en un estudio volumétrico realizado en primeros molares superiores humanos.
Hoikkala et al.(43) analizaron in vitro el comportamiento de diferentes VBa, especialmente el de las variedades 45S5 y S53P4 incorporados a la matriz de PDS de GuttaFlow® bioseal. El material que demostró las mejores condiciones de bioactividad en cuanto a su alcalinidad y la precipitación de óxidos de calcio y fósforo correspondió al compuesto 45S5/ PDS.
Accardo et al.(38) compararon in vitro la biocompatibilidad de GuttaFlow® bioseal, GuttaFlow® 2 y AH Plus® Jet (Dentsply, York, PA, Estados Unidos) en contacto con fibroblastos periodontales humanos mediante un ensayo de viabilidad y adhesión celular a los materiales y comprobaron que no hubo diferencias significativas entre las formulaciones de Gutta- Flow. Sin embargo, las diferencias fueron significativas con AH Plus® Jet.
Collado-González et al.(40) evaluaron in vitro la toxicidad de GuttaFlow® bioseal y GuttaFlow® 2 en comparación con MTA Fillapex y AHPlus en cultivos de células madre periodontales humanas en cuanto a su viabilidad y adhesión a los materiales ensayados. Luego de 24 horas, se observó un índice de viabilidad y de adhesión a GuttaFlow® bioseal y GuttaFlow® 2 significativamente superior a los otros dos materiales.
En un ensayo in vivo, Delfino et al.(37) implantaron muestras de GuttaFlow® bioseal, MTA Fillapex y EndoFill en tejido celular subcutáneo de ratas y analizaron el espesor de la cápsula fibrosa, la inflamación, la presencia de Interleukina 6 (IL-6), el factor de crecimiento endotelial y precipitaciones cálcicas distróficas durante 7, 15, 30 y 60 días. Al finalizar el ensayo, observaron que los índices de concentración de los factores investigados fueron superiores para GuttaFlow® bioseal y MTA Fillapex en comparación con EndoFill.
Bezerra da Silva et al.(41) compararon la biocompatibilidad de GuttaFlow® 2, Sealapex Xpress® y AH Plus® mediante implantes de los materiales en el tejido celular subcutáneo de ratones. Luego de 63 días, todos los materiales analizados fueron bien tolerados por los tejidos circundantes. Sin embargo, la biocompatibilidad de GuttaFlow® 2 resultó significativamente superior.
Washio et al.(44) analizaron las características del sellador Nishika Canal Sealer BG (Nippon Shika, Yakuhin Co, Yamaguchi, Japón) e informaron sobre su presentación en forma de dos pastas contenidas en una jeringa que permite dispensar su contenido en proporción 1:1. La pasta A está compuesta por ácidos grasos, subnitrato de bismuto y dióxido de silicio. La pasta B contiene óxido de magnesio, vidrio de silicato de calcio y dióxido de silicio. La reacción de fraguado se produce cuando la mezcla toma contacto con la humedad de la dentina. La biocompatibilidad del material fue analizada en un ensayo clínico en el que se obturaron conductos radiculares con gutapercha y el sellador NRCS en 127 piezas dentarias humanas.
El control posoperatorio fue realizado durante un periodo de 3 años al cabo del cual se observó que el 91% de los dientes persistieron en condiciones de normalidad clínica y radiográfica. El análisis de la evolución de 56 dientes correspondientes al ensayo fue realizado mediante el índice radiográfico periapical (PAI) demostrando un resultado satisfactorio. El 9% de los dientes fueron extraídos por causas no relacionadas al tratamiento endodóntico per se. Los autores concluyeron que el sellador investigado presenta condiciones clínicas favorables para la obturación del sistema de conductos radiculares. En otro ensayo clínico, Washio et al.(45) evaluaron el efecto del sellador sobre la incidencia de dolor posoperatorio luego del tratamiento endodóntico. Para ello, 4 endodoncistas y 7 odontólogos con experiencia endodóntica realizaron el tratamiento en 555 conductos radiculares pertenecientes a pacientes de ambos sexos de los cuales 122 fueron biopulpectomías (22%) y 433 fueron tratamientos en conductos con pulpas necróticas e infectadas (78%). Las obturaciones fueron realizadas con gutapercha y el sellador Nishika Canal Sealer BG. La percepción de diferentes grados de dolor se registró en 8 (1,5%) de las piezas dentarias tratadas, pero solamente durante los primeros 7 días posoperatorios. No hubo diferencias significativas respecto a dolor posoperatorio entre los casos de biopulpectomías o tratamiento en conductos infectados.
Elzubair et al.(46) analizaron el polímero termoplástico conocido comercialmente como Resilon ron que contiene VBa en forma de partículas como material de relleno. Por su parte, Marending et al.(47) describieron la formulación de Bio-Gutta, una gutapercha experimental que tiene incorporado Bioglass 45S5, lo que le permite adherirse a las paredes dentinarias y reduce significativamente la contracción que sufre la gutapercha cuando se reduce la temperatura inicial a la que fue termoplastizada. Las nuevas investigaciones que se encuentran actualmente en desarrollo permitirán obtener una mayor comprensión de los procesos de interacción de los VBa con el medio biológico con el que habitualmente se ponen en contacto.
Conclusión
Las investigaciones precedentes permiten sugerir que los excelentes resultados obtenidos con el uso de los VBa en el terreno de la endodoncia los hacen especialmente indicados para ser utilizados como materiales de protección pulpar directa y/o para la obturación del sistema de conductos radiculares. Sin embargo, debe quedar claro que en el presente trabajo sólo se analizaron los resultados de las experiencias que ensayan las propiedades biológicas y la bioactividad de los VBa. Por tal motivo, aún se requiere de una información más exhaustiva con respecto a sus propiedades fisicoquímicas y su influencia en la evolución clínica de los tratamientos.
Declaración de conflicto de intereses: El autor declara no tener conflicto de intereses en relación con este artículo científico.
Fuentes de financiamiento: Este estudio fue financiado exclusivamente por el autor.
Contacto:
Osvaldo Zmener
osvaldo@zmener.com.ar
Referencias
- Fernandes HR, Gaddam A, Rebelo A, Brazete D, Stan GE, Ferreira JMF. Bioactive glasses and glass-ceramics for health care applications in bone regeneration and tissue engineering. Materials 2018;11:2530. https://doi.org/10.3390/ma11122530
- Hench LL. Biomaterials: A forecast for the future. Biomaterials 1998;19:1419-23. https://doi.org/10.1016/s0142-9612(98)00133-1
- Boccaccini AR, Erol M, Stark WJ, Mohn D, Hong Z, Mano JF. Polymer/bioactive glass nano composites for medical applications: a review. Compos Sci Technol 2010;70:1764- 76. https://doi.org/10.1016/j.compscitech.2010.06.002
- Ali S, Farooq I, Iqbal K. A review of the effect of various ions on the properties and the clinical applications of novel bioactive glasses in medicine and dentistry. Saudi Dent J 2014;26:1-5. https://dx.doi.org/10.1016/j.sdentj.2013.12.001
- Xynos ID, Edgar AJ, Buttery LDK, Hench LL, Polak JM. Gene-expression profiling of human osteoblasts following treatment with the ionic products of Bioglass® 45S5 dissolution. J Biomed Mat Res 2001;55:151-7. https://doi.org/10.1002/1097-4636(200105)55:2%3C151::aid-jbm1001%3E3.0.co;2-d
- Sepulveda P, Jones J, Hench LL. In vitro dissolution of melt-derived 45S5 and sol-gel derived 58S bioactive glasses. J Biomed Mat Res 2002;61:301-11. https://doi.org/10.1002/jbm.10207
- Mena-Álvarez J, Rico-Romano C, Gutierrez-Ortega C, Arias-Sanz P, Castro-Urda J. A comparative study of biocompatibility in rat connective tissue of a new mineral trioxide compound (Theracal) versus MTA and a bioactive G3 glass. J Clin Med 2021;10:2536. https://doi.org/10.3390/jcm10122536
- Skallevold HE, Rokaya D, Khurshid Z, Zafar MS. Bioactive glass applications in dentistry. Int Mol Sci 2019;20:5960. https://doi.org/10.3390/ijms20235960
- ISO International Organization for standardization. 6876. Root canal sealing materials 6876, 2012[citado el 15 de diciembre de 2023]. Disponible en: https://www.iso.org/standard/45117.html
- Waltimo T, Brunner M, Vollenweider M, Stark WJ, Zehnder M. Antimicrobial effect of nanometric Bioactive Glass 45S5. J Dent Res 2007;86:754-7. https://doi.org/10.1177/154405910708600813
- Wang Y-Y, Chatsistavrou X, Faulk D, Badylak S, Zhang L, Papagerakis S, et al. Biological and bactericidal properties of Ag-doped bioactive glass in a natural extracelular matrix hydro gel with potential application in dentistry. Eur Cells Mater 2015;29:342-55. https://doi.org/10.22203/eCM.v029a26
- Allan I, Newman H, Wilson M. Antibacterial activity of particulate Bioglass® against supra-and subgingival bacteria. Biomaterials 2001;22:1683-7. https://doi.org/10.1016/s0142-9612(00)00330-6
- Mohn D, Bruhin C, Luechinger NA, Stark WJ, Imfeld T, Zehnder M. Composites made of flame sprayed bioactive glass 45S5 and polymers: bioactivity and immediate sealing properties. Int Endod J 2010;43:1037-46. https://doi.org/10.1111/j.1365-2591.2010.01772.x
- Mohn D, Zehnder M, Imfeld T, Stark WJ. Radio-opaque nanosized bioactive glass for potential root canal application: evaluation of radiopacity, bioactivity and alkaline capacity. Int Endod J 2010;43:210-7. https://doi.org/10.1111/j.1365-2591.2009.01660.x
- Pantchev A, Nohlert E, Tegelberg A. Endodontic surgery with and without inserts of bioactive glass PerioGlas® – a clinical and radiographic follow-up. Oral Maxillofac Surg 2009;13:21-6. https://doi.org/10.1007/s10006-008-0141-5
- Odatsu T, Azimaie T, Velten MF, Vu M, Lyles MB, Kim HK, et al. Human periosteum cell osteogenic differentiation enhanced by ionic silicon release from porous amorphous silica fibrous scaffolds. J Biomed Mat Res 2015;103:2797-806. https://doi.org/10.1002/jbm.a.35412
- Gholami S,Labbaf S, Houreh AB, Ting HK, Jones JR, Esfahani MAN. Long term effects of bioactive glass particulates on dental pulp stem cells in vitro. Biomed Glasses 2017;3:96-103. https://doi.org/10.1515/bglass-2017-0009
- Singh S, Patil A, Mali S, Jaiswal H. Bioglass: A new era in modern dentistry. Eur J Gen Dent 2022;11:1-6. https://doi.org/10.1055/s-0042-1742356
- Stoor P, Söderling E, Salonen JI. Antibacterial effects of bioactive glass paste on oral microorganisms. Acta Odontol Scand 1998;56:161-5. https://doi.org/10.1080/000163598422901
- Özer H, Özcan M. Antibacterial effect of bioactive glass incorporated in acrylic resins against Streptococcus mutans and Lactobacillus acidophilus activity in biofilm. Braz Dent Sci 2022;25:e3317. https://doi.org/10.4322/bds.2022.e3317
- Allan I, Wilson M, Newman H. Particulate Bioglass® reduces the viability of bacterial biofilms on its surface in an in vitro model. Clin Oral Implants Res 2002;13:53-8. https://doi.org/10.1034/j.1600-0501.2002.130106.x
- Zehnder M, Soderling E, Salonen J, Waltimo T. Preliminary evaluation of bioactive glass S53P4 as an endodontic medication in vitro. J Endod 2004;30:220-4. https://doi.org/10.1097/00004770-200404000-00009
- Zehnder M, Waltimo T, Sener B, Söderling E. Dentine enhances the effectiveness of bioactive glass S53P4 against a strain of Enterococcus faecalis. O Surg O Med O Pathol O Radiol Endod 2006;101:530-5. https://doi.org/10.1016/j.tripleo.2005.03.014
- Prabhakar AR, Kumar SCh. Antibacterial effect of bioactive glass in combination with powdered enamel and dentin. Indian J Dent Res 2010;21:30-4. https://doi.org/10.4103/0970-9290.62807
- Prasad SS, Ratha I, Adarsh T, Anand A, Sinha PK, Diwan P, et al. In vitro bioactivity and antibacterial properties of bismuth oxide modified bioactive glasses. J Mat Res 2018;33:178-90.https://doi.org/10.1557/jmr.2017.442
- Wilson J, Pigott GH, Schoen FJ, Hench LL. Toxicological and biocompatibility of bioglasses. J Biomed Res 1981;15:805-17. https://doi.org/10.1002/jbm.820150605
- Krishnan V, Lakshimi T. Bioglass: A novel biocompatible innovation. J Adv Pharm Technol Res 2013[citado el 15 de diciembre de 2023];4:78-83. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3696226/
- Oguntebi BR, Clark AE, Wilson J. Pulp capping with Bioglass ® and autologous demineralized dentin in miniatures swine. J Dent Res1993;72:484-9. https://doi.org/10.1177/00220345930720020301
- Oguntebi BR, Heaven T, Clark AE, Pink FE. Quantitative assessment of dentin bridge formation following pulp-capping in miniatures swine. J Endod 1995;21:79-82. https://doi.org/10.1016/S0099-2399(06)81100-3
- Long Y, Liu S, Zhu L, Liang Q, Chen X, Dong Y. Evaluation of pulp response to novel bioactive glass pulp capping materials. J Endod 2017;43:1647-50. https://doi.org/10.1016/j.joen.2017.03.011
- Hanada K, Morotomi T, Washio A, Yada N, Matsuo K, Teshima H. In vitro and in vivo effects of a novel bioactiveglass- based cement used as a direct pulp capping agent. J Biomed Mater Res B Appl Biomater 2019;107:161-8. https://doi.org/10.1002/jbm.b.34107
- Haghgoo R, Ahmadvant M. Evaluation of pulpal response of deciduous teeth after direct pulp capping with bioactive glass and mineral trioxide aggregate. Contemp Clin Dent 2016;7:332-5. https://doi.org/10.4103/0976-237X.188552
- Haghgoo R, Asgary S, Montazery R. Histopathological evaluation of primary teeth after pulp capping with calcium-enriched mixture and bioactive glass. Iranian Endod J 2018;13:457-60. https://doi.org/10.22037/iej.v13i4.20970
- Washio A, Morotomi T, Yoshii K, Kitamura Ch. Bioactive glass-based endodontic sealer as a promising root canal filling material without semisolid core materials. Materials (Basel) 2019;12:3967. https://doi.org/10.3390/ma12233967
- Rodriguez-Lozano FJ, Collado-González M, Tomas-Catalá CJ, García-Bernal D, López S, Oñate-Sánchez RE, et al. GuttaFlow Bioseal promotes spontaneous differentiation of human periodontal ligament stem cells into cementoblast- like cells. Dent Mater 2019;35:114-24. https://doi.org/10.1016/j.dental.2018.11.003
- Gandolfi MG, Siboni F, Prati C. Properties of a novel polysiloxane-guttapercha calcium silicate-bioglass-containing root canal sealer. Dent Mater 2016;32:113-26. https://doi.org/10.1016/j.dental.2016.03.001
- Delfino MM, Guerreiro-Tanomaru JM, Tanomaru-Filho M, Sasso-Cerri E, Cerri PS. Immunoinflammatory response and bioactive potential of GuttaFlow bioseal and MTA Fillapex in the rat subcutaneous tissue. Sci Rep 2020;10:7173. https://doi.org/10.1038/s41598-020-64041-0
- Accardo C, Himel VT, Lallier TE. A novel GuttaFlow sealer supports cell survival and attachment. J Endod 2014;40:231-4. https://doi.org/10.1016/j.joen.2013.08.029
- Willershausen I, Callaway A, Briseño B, Willershausen B. In vitro analysis of the cytotoxicity and the antimicrobial effect of four endodontic sealers. Head Face Med 2011;7:15. https://doi.org/10.1186/1746-160X-7-15
- Collado-González M, Tomás-Catalá J, Oñate-Sánchez RE, Moraleda JM, Rodríguez-Lozano J. Cytotoxicity of GuttaFlow Bioseal, GuttaFlow2, MTA Fillapex, and AHPlus on human periodontal ligament stem cells. J Endod 2017;43:816-22. https://doi.org/10.1016/j.joen.2017.01.001
- Bezerra da Silva LA, Bertasso AS, Pucinelly CM, Bezerra da Silva RA, de Oliveira KMH, Sousa-Neto MD, et al. Novel endodontic sealers induced satisfactory tissue response in mice. Biomed Pharmacother 2018;106:1506-12. https://doi.org/10.1016/j.biopha.2018.07.065
- Zhong X, Shen Y, Ma J, Chen W-X, Haapasalo M. Quality of root filling after obturation with gutta-percha and 3 different sealers of minimally instrumented root canals in the maxillary first molar. J Endod 2019;45:1030-5. https://doi.org/10.1016/j.joen.2019.04.012
- Hoikkala NPJ, Siekkinen M, Hupa L, Vallittu PK. Behaviour of different bioactive glasses incorporated in polydimethylsiloxane endodontic sealer. Dent Mater 2021;37:321-7. https://doi.org/10.1016/j.dental.2020.11.013
- Washio A, Miura H, Suematsu M, Murata K, Aihara R, Fujimoto M, et al. Three-year retrospective follow-up of cases of root canal obturation with a bioactiveglass-based root canal sealer. Oper Dent Endodontology Periodon 2022;2:16-24. https://doi.org/10.11471/odep.2022-003
- Washio A, Miura H, Morotomi T, Suematsu MI, Miyahara H, Hanada-Miyahara K, et al. Effect of bioactive glass-based root canal sealer on the incidence of postoperative pain after root canal obturation. Int J Environ Res Public Health 2020;17:8857. https://doi.org/10.3390/ijerph17238857
- Elzubair A, Elías CN, Suárez JCM, Lopez HP, Vieira MVB. The physical characterization of a thermoplastic polymerfor endodontic obturation. J Dent 2006;34:784-9. https://doi.org/10.1016/j.jdent.2006.03.002
- Marending M, Buberhofer SB, Sener B, De-Deus G. Primary assessment of a self-adhesive gutta-percha material. Int Endod J 2013;46:317-22. https://doi.org/10.1111/j.1365-2591.2012.02117.x
Biocompatibilidad Bioglass® hidroxiapatita vidrio bioactivo Bioactive glass biocompatibility Bioglass hydroxyapatite
Citar este artículo
Zmener O. Vidrios bioactivos en endodoncia. Revisión narrativa de sus propiedades biológicas. Rev Asoc Odontol Argent. 2024-Mar-15;112(1):e1120451. https://doi.org/10.52979/raoa1120451.1248
Copiar Cita
PDF | Subir | Home
X Twitter | WhatsApp | Facebook | E-mail
Las obras publicadas en este sitio están bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional
Revista indexada en:













Los artículos científicos de RAOA se identifican con DOI (Digital Object Identifier) Crossref.
Visitas al artículo: 420

Lecturas en línea: 375

Descargas del artículo: 45

Accesos por DOI: 85

Database ID: 2024005002
Auspiciantes del Website:







Revista de la Asociación Odontológica Argentina
La Revista de la Asociación Odontológica Argentina, RAOA, es la principal vía de expresión de la producción científica argentina en odontología y un vínculo de unión y medio de información para los colegas e instituciones del país y del exterior.
Versión impresa ISSN 0004-4881
Versión electrónica ISSN 2683-7226.
DOI: 10.52979/raoa.1898
Título abreviado: Rev Asoc Odontol Argent

